ūŽ═Ō╬³╩š╣ŌūVĄ─╗∙▒ŠįŁ└Ē
╬³╩š╣ŌūVĄ─«a(ch©Żn)╔·
įSČÓ¤o╔½═Ė├„Ą─ėąÖC(j©®)╗»║Ž╬’Ż¼ļm▓╗╬³╩š┐╔ęŖ╣ŌŻ¼Ą½═∙═∙─▄╬³╩šūŽ═Ō╣ŌĪŻ╚ń╣¹ė├ę╗╩°Š▀ėą▀B└m(x©┤)▓©ķLĄ─ūŽ═Ō╣Ōšš╔õėąÖC(j©®)╗»║Ž╬’Ż¼▀@Ģr(sh©¬)ūŽ═Ō╣Ōųą─│ą®▓©ķLĄ─╣Ō▌Ś╔õŠ═┐╔ęį▒╗įō╗»║Ž╬’Ą─Ęųūė╦∙╬³╩šŻ¼╚¶īó▓╗═¼▓©ķLĄ─╬³╩š╣ŌČ╚ėøõøŽ┬üĒŻ¼Š═┐╔½@Ą─įō╗»║Ž╬’Ą─ūŽ═Ō╬³╩š╣ŌūV.
ūŽ═Ō╣ŌūVĄ─▒Ē╩ŠĘĮĘ©
═©│Żęį▓©ķL”╦×ķÖM▌SĪó╬³╣ŌČ╚AŻ©░┘Ęų═Ė╣Ō┬╩T%Ż®×ķ┐v▌Sū„łDŻ¼Š═┐╔½@Ą─įō╗»║Ž╬’Ą─ūŽ═Ō╬³╩š╣ŌūVłDĪŻ
╬³╣ŌČ╚AŻ¼▒Ē╩Šå╬╔½╣Ō═©▀^─│ę╗śėŲĘĢr(sh©¬)▒╗╬³╩šĄ─│╠Č╚ A=log(I0/I1), I0╚ļ╔õ╣ŌÅŖ(qi©óng)Č╚Ż¼I1═Ė▀^╣ŌÅŖ(qi©óng)Č╚Ż╗
═Ė╣Ō┬╩ę▓ĘQ═Ė╔õ┬╩TŻ¼×ķ═Ė▀^╣ŌÅŖ(qi©óng)Č╚I1┼c╚ļ╔õ╣ŌÅŖ(qi©óng)Č╚I0ų«▒╚ųĄŻ¼T= I1/I0═Ė╣Ō┬╩T┼c╬³╣ŌČ╚AĄ─ĻP(gu©Īn)ŽĄ×ķ A=log(1/T)
Ė∙ō■(j©┤)└╩▓«-▒╚Ā¢Č©┬╔Ż¼╬³╣ŌČ╚A┼c╚▄ę║ØŌČ╚c│╔š²▒╚ A=”┼bc ”┼×ķ─”Ā¢╬³╣ŌŽĄöĄ(sh©┤)Ż¼╦³╩ŪØŌČ╚×ķ1mol/LĄ─ ╚▄ę║į┌1cmĄ─╬³╩š│žųąŻ¼į┌ę╗Č©▓©ķLŽ┬£yĄ├Ą─╬³╣ŌČ╚Ż¼╦³▒Ē╩Š╬’┘|(zh©¼)ī”(du©¼)╣Ō─▄Ą─╬³╩šÅŖ(qi©óng)Č╚Ż¼╩ŪĖ„ĘN╬’┘|(zh©¼)į┌ę╗Č©▓©ķLŽ┬Ą─╠žš„│ŻöĄ(sh©┤)Ż¼ę“Č°╩ŪÖzČ©╗»║Ž╬’Ą─ųžę¬öĄ(sh©┤)ō■(j©┤)Ż╗c×ķ╬’┘|(zh©¼)Ą─ØŌČ╚Ż¼å╬╬╗×ķmol/LŻ╗b×ķę║īė║±Č╚Ż¼å╬╬╗×ķcmĪŻ
į┌ūŽ═Ō╬³╩š╣ŌūVųą│Żęį╬³╩šÄ¦ūŅ┤¾╬³╩š╠Ä▓©ķL”╦max║═įō▓©ķLŽ┬Ą──”Ā¢╬³╩šŽĄöĄ(sh©┤)”┼maxüĒ▒Ēš„╗»║Ž╬’╬³╩š╠žš„ĪŻ╬³╩š╣ŌūVĘ┤ė│┴╦╬’┘|(zh©¼)Ęųūėī”(du©¼)▓╗═¼▓©ķLūŽ═Ō╣ŌĄ─╬³╩š─▄┴”ĪŻ╬³╩šÄ¦Ą─ą╬ĀŅĪó”╦max║═”┼max┼c╬³╣ŌĘųūėĄ─ĮY(ji©”)śŗ(g©░u)ėą├▄ŪąĄ─ĻP(gu©Īn)ŽĄĪŻĖ„ĘNėąÖC(j©®)╗»║Ž╬’Ą─”╦max║═”┼maxČ╝ėąČ©ųĄŻ¼═¼ŅÉ╗»║Ž╬’Ą─”┼max▒╚▌^ĮėĮ³Ż¼╠Äė┌ę╗éĆ(g©©)ĘČć·ĪŻ
ūŽ═Ō╬³╩š╣ŌūV╩Ūė╔Ęųūėųąār(ji©ż)ļŖūė─▄╝ē(j©¬)▄S▀w╦∙«a(ch©Żn)╔·Ą─ĪŻė╔ė┌ļŖūė─▄╝ē(j©¬)▄S▀w═∙═∙ę¬ę²ŲĘųūėųą║╦Ą─▀\(y©┤n)äė(d©░ng)ĀŅæB(t©żi)Ą─ūā╗»Ż¼ę“┤╦į┌ļŖūė▄S▀wĄ─═¼Ģr(sh©¬)Ż¼┐é╩Ū░ķļSų°ĘųūėĄ─š±äė(d©░ng)─▄╝ē(j©¬)║═▐D(zhu©Żn)äė(d©░ng)─▄╝ē(j©¬)Ą─▄S▀wĪŻ┐╝æ]▄S▀wŪ░Ą─╗∙æB(t©żi)Ęųūė▓ó▓╗╩Ū╚½╩Ū╠Äė┌ūŅĄ═š±äė(d©░ng)║═▐D(zhu©Żn)äė(d©░ng)─▄╝ē(j©¬)Ż¼Č°╩ŪĘų▓╝į┌╚¶Ė╔▓╗═¼Ą─š±äė(d©░ng)║═▐D(zhu©Żn)äė(d©░ng)─▄╝ē(j©¬)╔ŽŻ╗Č°ŪęļŖūė▄S▀w║¾Ą─Ęųūėę▓▓╗╚½╠Äė┌╝ż░l(f©Ī)æB(t©żi)Ą─ūŅĄ═š±äė(d©░ng)║═▐D(zhu©Żn)äė(d©░ng)─▄╝ē(j©¬)Ż¼Č°╩Ū┐╔▀_(d©ó)ĄĮ▌^Ė▀Ą─š±äė(d©░ng)║═▐D(zhu©Żn)äė(d©░ng)─▄╝ē(j©¬),ę“┤╦ļŖūė─▄╝ē(j©¬)▄S▀w╦∙«a(ch©Żn)╔·Ą─╬³╩šŠĆė╔ė┌ĖĮ╝ė╔Žš±äė(d©░ng)─▄╝ē(j©¬)║═▐D(zhu©Żn)äė(d©░ng)─▄╝ē(j©¬)Ą─▄S▀wČ°ūā│╔īÆĄ─╬³╩šÄ¦ĪŻ┤╦═ŌŻ¼▀M(j©¼n)ąąūŽ═Ō╣ŌūV£yČ©Ģr(sh©¬)Ż¼┤¾ČÓöĄ(sh©┤)▓╔ė├ę║¾w╗“╚▄ę║įćśėĪŻę║¾wųą▌^ÅŖ(qi©óng)Ą─Ęųūėķgū„ė├┴”Ż¼╗“╚▄ę║ųąĄ─╚▄ä®╗»ū„ė├Č╝ī¦(d©Żo)ų┬š±äė(d©░ng)Īó▐D(zhu©Żn)äė(d©░ng)Š½╝Ü(x©¼)ĮY(ji©”)śŗ(g©░u)Ą─Ž¹╩¦ĪŻĄ½╩Ūį┌ę╗Č©Ą─Śl╝■Ž┬Ż¼╚ńĘŪśOąį╚▄䮥─ŽĪ╚▄ę║╗“ÜŌ¾wĀŅæB(t©żi)Ż¼╚į┐╔ė^▓ņĄĮūŽ═Ō╬³╩š╣ŌūVĄ─š±äė(d©░ng)╝░▐D(zhu©Żn)äė(d©░ng)Š½╝Ü(x©¼)ĮY(ji©”)śŗ(g©░u)ĪŻ
Ęųūė▄ēĄ└┼cļŖūė▄S▀wĄ─ŅÉą═
Ęųūė▄ēĄ└╗∙▒ŠįŁ└Ē
Ė∙ō■(j©┤)Ęųūė▄ēĄ└└ĒšōŻ¼«ö(d©Īng)2éĆ(g©©)įŁūėą╬│╔╗»īW(xu©”)µIĢr(sh©¬)Ż¼įŁūė▄ēĄ└īó▀M(j©¼n)ąąŠĆąįĮM║Žą╬│╔Ęųūė▄ēĄ└ĪŻĘųūė▄ēĄ└Š▀ėąĘųūėĄ─š¹¾wąįŻ¼╦³īó2éĆ(g©©)įŁūėū„×ķš¹¾w┬ō(li©ón)ŽĄį┌ę╗ŲŻ¼ą╬│╔Ą─Ęųūė▄ēĄ└öĄ(sh©┤)Ą╚ė┌╦∙ĮM║ŽĄ─įŁūė▄ēĄ└öĄ(sh©┤)ĪŻ└²╚ńā╔éĆ(g©©)═Ōīėų╗ėą1éĆ(g©©)SļŖūėĄ─įŁūėĮY(ji©”)║Ž│╔ĘųūėĢr(sh©¬)Ż¼ā╔éĆ(g©©)įŁūė▄ēĄ└┐╔ęįŠĆąįĮM║Žą╬│╔ā╔éĆ(g©©)Ęųūė▄ēĄ└Ż¼Ųõųąę╗éĆ(g©©)Ęųūė▄ēĄ└Ą──▄┴┐▒╚ŽÓæ¬(y©®ng)Ą─įŁūė▄ēĄ└─▄┴┐Ą═Ż¼ĘQ×ķ│╔µIĘųūė▄ēĄ└Ż╗┴Ēę╗éĆ(g©©)Ęųūė▄ēĄ└Ą──▄┴┐▒╚ŽÓæ¬(y©®ng)Ą─įŁūė▄ēĄ└─▄┴┐Ė▀Ż¼ĘQ×ķĘ┤µIĘųūė▄ēĄ└Ż©Ę┤µI▄ēĄ└│Żė├*ś╦(bi©Īo)│÷Ż®ĪŻ
Ęųūė▄ēĄ└ųąūŅ│ŻęŖĄ─ėą”ę▄ēĄ└║═”ą▄ēĄ└ā╔ŅÉĪŻ”ę▄ēĄ└╩ŪįŁūė═ŌīėĄ─S▄ēĄ└┼cS▄ēĄ└Īó╗“Px▄ēĄ└┼cPx▄ēĄ└Ż©čž”ų▌S┐┐Į³Ģr(sh©¬)Ż®ŠĆąįĮM║Žą╬│╔Ą─Ęųūė▄ēĄ└ĪŻ│╔µI”ęĘųūė▄ēĄ└Ą─ļŖūėįŲĘų│╩łAų∙ą═ī”(du©¼)ĘQŻ¼ļŖūėįŲ├▄╝»ė┌ā╔įŁūė║╦ų«ķgŻ╗Č°Ę┤µI”ęĘųūė▄ēĄ└Ą─ļŖūėįŲį┌įŁūė║╦ų«ķgĄ─Ęų▓╝▒╚▌^ŽĪ╩ĶŻ¼╠Äė┌│╔µI”ę▄ēĄ└╔ŽĄ─ļŖūėĘQ×ķ│╔µI”ęļŖūėŻ¼╠Äė┌Ę┤µI”ę▄ēĄ└╔ŽĄ─ļŖūėĘQ×ķĘ┤µI”ęļŖūėĪŻ”ą▄ēĄ└╩ŪįŁūėūŅ═ŌīėPy▄ēĄ└╗“Pz▄ēĄ└Ż©čž”ų▌S┐┐Į³Ģr(sh©¬)Ż®ŠĆąįĮM║Žą╬│╔Ą─Ęųūė▄ēĄ└ĪŻ│╔µI”ąĘųūė▄ēĄ└Ą─ļŖūėįŲĘų▓╗│╩łAų∙ą═ī”(du©¼)ĘQŻ¼Ą½ėąę╗ī”(du©¼)ī”(du©¼)ĘQŻ¼į┌┤╦ŲĮ├µ╔ŽļŖūėįŲ├▄Č╚Ą╚ė┌┴ŃŻ¼Č°ī”(du©¼)ĘQ├µĄ─╔ŽŽ┬▓┐┐šķgät╩ŪļŖūėįŲĘų▓╝Ą─ų„ę¬ģ^(q©▒)ė“ĪŻĘ┤µI”ąĘųūė▄ēĄ└Ą─ļŖūėįŲę▓ėąę╗ī”(du©¼)ĘQ├µŻ¼Ą½2éĆ(g©©)įŁūėĄ─ļŖūėįŲ╗źŽÓĘųļxŻ¼╠Äė┌│╔µI”ą▄ēĄ└Ą─ļŖūėĘQ×ķ│╔µI”ąļŖūėŻ¼╠Äė┌Ę┤µI”ą▄ēĄ└Ą─ļŖūėĘQ×ķĘ┤µI”ąļŖūėĪŻ
║¼ėąč§ĪóĄ¬Īó┴“Ą╚įŁūėĄ─ėąÖC(j©®)╗»║Ž╬’ĘųūėųąŻ¼▀Ć┤µį┌╬┤ģó┼c│╔µIĄ─ļŖūėī”(du©¼)Ż¼│ŻĘQ×ķ╣┬ī”(du©¼)ļŖūėĪŻ╣┬ī”(du©¼)ļŖūė╩ŪĘŪµIļŖūėŻ¼ę▓ĘQ×ķnļŖūėĪŻ└²╚ń╝ū┤╝ĘųūėųąĄ─č§įŁūėŻ¼Ųõ═Ōīėėą6éĆ(g©©)ļŖūėŻ¼Ųõųą2éĆ(g©©)ļŖūėĘųäe┼c╠╝įŁūė║═ÜõįŁūėą╬│╔2éĆ(g©©)”ęµIŲõėÓ4éĆ(g©©)ļŖūė▓ó╬┤ģó┼c│╔µIŻ¼╚į╠Äė┌įŁūė▄ēĄ└╔ŽŻ¼ĘQ×ķnļŖūėĪŻČ°nļŖūėĄ─įŁūė▄ēĄ└ĘQ×ķn▄ēĄ└ĪŻ
ļŖūė▄S▀wĄ─ŅÉą═
Ė∙ō■(j©┤)Ęųūė▄ēĄ└Ą─ėŗ(j©¼)╦ŃĮY(ji©”)╣¹Ż¼Ęųūė▄ēĄ└─▄╝ē(j©¬)Ą──▄┴┐ęįĘ┤µI”ę▄ēĄ└ūŅĖ▀Ż¼Č°n▄ēĄ└Ą──▄┴┐Įķė┌│╔µI▄ēĄ└┼cĘ┤µI▄ēĄ└ų«ķgĪŻĘųūė▄ēĄ└─▄╝ē(j©¬)Ą─Ė▀Ą═┤╬ą“╚ńŽ┬Ż║
”ę*>”ą*>n>”ą>”ę
ļŖūė▄S▀wĘĮ╩Įų„ę¬ėą4ĘN╚ńłD1╦∙╩Š
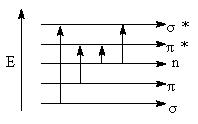
łD1”ęĪó”ąĪón▄ēĄ└╝░ļŖūė▄S▀w
1Īó”ę ”ę* ”ęµIµI─▄Ė▀Ż¼ę¬╩╣”ęļŖūė▄S▀wąĶę¬║▄Ė▀Ą──▄┴┐Ż¼┤¾╝s780KJ.mol-1Ż¼╩Ūę╗ĘNĖ▀─▄▄S▀wĪŻ▀@ŅÉ▄S▀wī”(du©¼)æ¬(y©®ng)Ą─╬³╩š▓©ķLČ╝į┌šµ┐šūŽ═Ōģ^(q©▒)Ż¼į┌Į³ūŽ═Ōģ^(q©▒)╩Ū═Ė├„Ą─Ż¼╦∙ęį│Żė├ū„£yČ©ūŽ═Ō╬³╩š╣ŌūVĄ─╚▄ä®ĪŻ
2Īó n ”ę* Ęųūėųą║¼ėąč§ĪóĄ¬Īó┴“Īó¹u╦žĄ╚įŁūėŻ¼ät«a(ch©Żn)╔·▀@ĘN▄S▀wŻ¼╦³▒╚”ę ”ę* ▄S▀wĄ──▄┴┐Ą═Ą├ČÓĪŻŻ©╝ū┴“┤╝ 227nmŻ¼ĄŌ╝ū═ķ258nmŻ®
3Īó”ą ”ą* ▓╗’¢║═╗»║Ž╬’╝░Ę╝ŽŃ╗»║Ž╬’│²║¼”ęļŖūė═ŌŻ¼▀Ć║¼ėą”ąļŖūėĪŻ”ąļŖūė╚▌ęū╩▄╝ż░l(f©Ī)Ż¼ļŖūėÅ─│╔µIĄ─”ą▄ēĄ└▄S▀wĄĮĘ┤µIĄ─”ą▄ēĄ└╦∙ąĶĄ──▄┴┐▒╚▌^Ą═ĪŻę╗░Ń╣┬┴óļpµIĄ─ęꎮĪó▒¹Ž®Ą╚╗»║Ž╬’Ż¼Ųõ”ą ”ą* ▄S▀wĄ─▓©ķLį┌170-200nmĘČć·ā╚(n©©i)Ż¼Ą½╬³╩šÅŖ(qi©óng)Č╚ÅŖ(qi©óng)Ż©104Ż®ĪŻ╚ń╣¹Ž®¤N╔Žėą╚Ī┤·╗∙╗“Ž®µI┼cŲõ╦³ļpµI╣▓▄ŚŻ¼”ą ”ą*▄S▀wĄ─╬³╩š▓©ķLīó╝tęŲĄĮĮ³ūŽ═Ōģ^(q©▒)ĪŻĘ╝ŽŃūÕ╗»║Ž╬’┤µį┌Łh(hu©ón)ĀŅĄ─╣▓▄Ś¾wŽĄŻ¼”ą ”ą* ▄S▀wĢ■(hu©¼)│÷¼F(xi©żn)╚²éĆ(g©©)╬³╩šÄ¦╝┤E╬³╩šÄ¦ĪóK╬³╩šÄ¦ĪóB╬³╩šÄ¦Ż©▒ĮŻ║184nmĪó203nmĪó256nmŻ®ĪŻ
4Īó n ”ą* «ö(d©Īng)╗»║Ž╬’Ęųūėųą═¼Ģr(sh©¬)║¼ėą”ąļŖūė║═nļŖūėät┐╔«a(ch©Żn)╔·▀@ĘN▄S▀wŻ¼n ”ą* Ż¼╦∙ąĶĄ──▄┴┐ūŅĄ═Ż¼Ųõ╦∙«a(ch©Żn)╔·Ą─╬³╩š▓©ķLūŅķLŻ¼Ą½╬³╩šÅŖ(qi©óng)Č╚║▄╚§Ż©▒¹═¬Ż║280nmŻ¼15Ż®ĪŻ
ļŖūė▄S▀wŅÉą═┼cĘųūėĮY(ji©”)śŗ(g©░u)╝░Ųõ┤µį┌Ą─╗∙łF(tu©ón)ėą├▄ŪąĄ─ĻP(gu©Īn)ŽĄ,┐╔ęįĖ∙ō■(j©┤)ĘųūėĮY(ji©”)śŗ(g©░u)üĒŅA(y©┤)£y┐╔─▄Ą─ļŖūė▄S▀wŻ©’¢║═¤N ”ę ”ę* Ż¼Ž®¤N ”ę ”ę*Īó”ą ”ą*Ż¼ ų¼ĘŠ├č”ę ”ę*Īón ”ę*Ż¼╚®═¬ ”ą ”ą* Īó n ”ę* Īó
”ę ”ę* Īó n ”ą*Ż®ĪŻ
░l(f©Ī)╔½╗∙łF(tu©ón)Īóų·╔½╗∙łF(tu©ón)║═╬³╩šÄ¦
Ż©1Ż®░l(f©Ī)╔½╗∙łF(tu©ón)║═ų·╔½╗∙łF(tu©ón)
░l(f©Ī)╔½╗∙łF(tu©ón) ─▄╩╣╗»║Ž╬’│÷¼F(xi©żn)Ņü╔½Ą─ę╗ą®╗∙łF(tu©ón)ĪŻį┌ūŽ═Ō╬³╩š╣ŌūVųąčžė├▀@ę╗ąg(sh©┤)šZŻ¼Ųõ║¼┴xęčĮø(j©®ng)öU(ku©░)│õĄĮĘ▓╩Ū─▄ī¦(d©Żo)ų┬╗»║Ž╬’į┌ūŽ═Ō╝░┐╔ęŖ╣Ōģ^(q©▒)«a(ch©Żn)╔·╬³╩šĄ─╗∙łF(tu©ón)Ż¼▓╗šō╩Ūʱ’@╩ŠŅü╔½Č╝ĘQ×ķ░l(f©Ī)╔½╗∙łF(tu©ón)ĪŻę╗░Ń▓╗’¢║═Ą─╗∙łF(tu©ón)Č╝╩Ū░l(f©Ī)╔½╗∙łF(tu©ón)Ż©C=CĪóC=OĪóN=N Īó╚²µIĪó▒ĮŁh(hu©ón)Ą╚Ż®ĪŻ
╚ń╣¹╗»║Ž╬’ųąėąÄūéĆ(g©©)░l(f©Ī)╔½╗∙łF(tu©ón)ŽÓ╗ź╣▓▄ŚŻ¼ätĖ„éĆ(g©©)░l(f©Ī)╔½╗∙łF(tu©ón)╦∙«a(ch©Żn)╔·Ą─╬³╩šÄ¦īóŽ¹╩¦Ż¼Č°╚Ī┤·│÷¼F(xi©żn)ą┬Ą─╣▓▄Ś╬³╩šÄ¦Ż¼Ųõ▓©ķLīó▒╚å╬éĆ(g©©)░l(f©Ī)╔½╗∙łF(tu©ón)Ą─╬³╩š▓©ķLķLŻ¼╬³╩šÅŖ(qi©óng)Č╚ę▓’@ų°╝ėÅŖ(qi©óng)ĪŻ
ų·╔½╗∙łF(tu©ón) įńŲ┌ę²╚ļĄ─ę╗éĆ(g©©)ąg(sh©┤)šZŻ¼╦³╩ŪųĖ─Ūą®▒Š╔Ē▓╗Ģ■(hu©¼)╩╣╗»║Ž╬’Ęųūė«a(ch©Żn)╔·Ņü╔½╗“š▀į┌ūŽ═Ō╝░┐╔ęŖ╣Ōģ^(q©▒)▓╗«a(ch©Żn)╔·╬³╩šĄ─ę╗ą®╗∙łF(tu©ón)Ż¼Ą½▀@ą®╗∙łF(tu©ón)┼c░l(f©Ī)╔½╗∙łF(tu©ón)ŽÓ▀BĢr(sh©¬)ģs─▄╩╣░l(f©Ī)╔½╗∙łF(tu©ón)Ą─╬³╩šÄ¦▓©ķLęŲŽ“ķL▓©Ż¼═¼Ģr(sh©¬)╩╣╬³╩šÅŖ(qi©óng)Č╚į÷╝ėĪŻ═©│ŻŻ¼ų·╔½╗∙łF(tu©ón)╩Ūė╔║¼ėą╣┬ī”(du©¼)ļŖūėĄ─į¬╦ž╦∙ĮM│╔Ż©-NH2 , -NR2 , -OH , -OR , -ClĄ╚Ż®Ż¼▀@ą®╗∙łF(tu©ón)ĮĶų·P-”ą╣▓▄Ś╩╣░l(f©Ī)╔½╗∙łF(tu©ón)į÷╝ė╣▓▄Ś│╠Č╚Ż¼Å─Č°╩╣ļŖūė▄S▀wĄ──▄┴┐Ž┬ĮĄĪŻ
Ė„ĘNų·╔½╗∙łF(tu©ón)Ą─ų·╔½ą¦æ¬(y©®ng)Ė„▓╗ŽÓ═¼Ż¼ęįO- ×ķūŅ┤¾Ż¼F×ķūŅąĪĪŻų·╔½╗∙łF(tu©ón)Ą─ų·╔½ą¦æ¬(y©®ng)ÅŖ(qi©óng)╚§┤¾ų┬╚ńŽ┬┴ąĒśą“ĪŻ
F < CH3 <Cl < Br < OH < SH < OCH3 <NH2 <NHR < NR2 < O-
Ż©Č■Ż®╝tęŲĪó╦{(l©ón)ęŲĪóį÷╔½ą¦æ¬(y©®ng)║═£p╔½ą¦æ¬(y©®ng)
ė╔ė┌ėąÖC(j©®)╗»║Ž╬’Ęųūėųąę²╚ļ┴╦ų·╔½╗∙łF(tu©ón)╗“Ųõ╦¹░l(f©Ī)╔½╗∙łF(tu©ón)Č°«a(ch©Żn)╔·ĮY(ji©”)śŗ(g©░u)Ą─Ė─ūāŻ¼╗“š▀ė╔ė┌╚▄䮥─ė░Ēæ╩╣ŲõūŽ═Ō╬³╩šÄ¦Ą─ūŅ┤¾╬³╩š▓©ķLŽ“ķL▓©ĘĮŽ“ęŲäė(d©░ng)Ą─¼F(xi©żn)Ž¾ĘQ×ķ╝tęŲĪŻ┼c┤╦ŽÓĘ┤Ż¼╚ń╣¹╬³╩šÄ¦Ą─ūŅ┤¾╬³╩š▓©ķLŽ“Č╠▓©ĘĮŽ“ęŲäė(d©░ng)Ż¼ätĘQ×ķ╦{(l©ón)ęŲĪŻ
┼c╬³╩šÄ¦▓©ķL╝tęŲ╝░╦{(l©ón)ęŲŽÓ╦ŲŻ¼ė╔ė┌╗»║Ž╬’ĘųūėĮY(ji©”)śŗ(g©░u)ųąę²╚ļ╚Ī┤·╗∙╗“╩▄╚▄䮥─ė░ĒæŻ¼╩╣╬³╩šÄ¦Ą─ÅŖ(qi©óng)Č╚╝┤─”Ā¢╬³╣ŌŽĄöĄ(sh©┤)į÷┤¾╗“£p╔┘Ą─ŽļŽ¾ĘQ×ķį÷╔½ą¦æ¬(y©®ng)╗“£p╔½ą¦æ¬(y©®ng)ĪŻ
Ż©╚²Ż® ╬³╩šÄ¦
į┌╦─ĘNļŖūė▄S▀wŅÉą═ųąŻ¼”ę ”ę*▄S▀w║═n ”ę*▄S▀w╔Ž«a(ch©Żn)╔·Ą─╬³╩šÄ¦▓©ķL╠Äė┌šµ┐šūŽ═Ōģ^(q©▒)ĪŻ”ą ”ą*▄S▀w║═n ”ą*▄S▀w╦∙«a(ch©Żn)╔·Ą─╬³╩šÄ¦│²─│ą®╣┬┴óļpµI╗»║Ž╬’═ŌŻ¼ę╗░ŃČ╝╠Äė┌Į³ūŽ═Ōģ^(q©▒)Ż¼╦³éā╩ŪūŽ═Ō╬³╩š╣ŌūV╦∙蹊┐Ą─ų„ę¬╬³╩šÄ¦ ĪŻ
ė╔”ą ”ą* ▄S▀w║═n ”ą*▄S▀w╦∙«a(ch©Żn)╔·Ą─╬³╩šÄ¦┐╔Ęų×ķŽ┬╩÷╦─ĘNŅÉą═
1ĪóR╬³╩šÄ¦ ė╔║¼ėąč§Īó┴“Ī󥬥╚ļsįŁūėĄ─░l(f©Ī)╔½╗∙łF(tu©ón)Ż©¶╩╗∙ĪóŽ§╗∙Ż®n ”ą*▄S▀w╦∙«a(ch©Żn)╔·Ż¼ ╬³╩š▓©ķLķLŻ¼╬³╩šÅŖ(qi©óng)Č╚Ą═Ż©ęę╚® 290nmŻ¼17Ż®ĪŻ
2Īó K╬³╩šÄ¦ ė╔║¼ėą╣▓▄ŚļpµIŻ©ČĪČ■Ž®Īó▒¹Ž®╚®Ż®Ą─”ą ”ą*▄S▀w╦∙«a(ch©Żn)╔·Ż¼K╬³╩šÄ¦▓©ķL┤¾ė┌200nmŻ¼╬³╩šÅŖ(qi©óng)Č╚ÅŖ(qi©óng)Ż©104Ż®ĪŻ
3Īó B╬³╩šÄ¦ ╩Ūķ]║ŽŁh(hu©ón)ĀŅ╣▓▄ŚļpµIĄ─”ą ”ą*▄S▀w╦∙«a(ch©Żn)╔·Ą─Ż¼╩ŪĘ╝Łh(hu©ón)╗»║Ž╬’Ą─ų„ę¬╠žš„╬³╩šĘÕĪŻ╬³╩š▓©ķLķLŻ¼╬³╩šÅŖ(qi©óng)Č╚Ą═Ż©▒Į 256nmŻ¼215Ż®ĪŻį┌ĘŪśOąį╚▄ä®ųą╗“ÜŌæB(t©żi)Ģr(sh©¬)Ż¼B╬³╩š┤¾Ä¦Ģ■(hu©¼)│÷¼F(xi©żn)Š½╝Ü(x©¼)ĮY(ji©”)śŗ(g©░u)Ż¼Ą½ėąę╗ą®Ę╝ŽŃ╗»║Ž╬’Ą─B╬³╩šÄ¦═∙═∙ø]ėąŠ½╝Ü(x©¼)ĮY(ji©”)śŗ(g©░u)Ż¼śOąį╚▄䮥─╩╣ė├Ģ■(hu©¼)╩╣Š½╝Ü(x©¼)ĮY(ji©”)śŗ(g©░u)Ž¹╩¦ĪŻ
4Īó E╬³╩šÄ¦ Ę╝ŽŃ╗»║Ž╬’Ą─╠žš„╬³╩šÄ¦Ż¼ėąā╔éĆ(g©©)╬³╩šĘÕŻ¼Ęųäe×ķE1Ħ║═E2ĦŻ¼E1Ą─╬³╩š╝sį┌180nmŻ©”┼ŻŠ104Ż®Ż¼E2Ą─╬³╩š╝sį┌200nmŻ©”┼=7000Ż®Ż¼Č╝╩ŪÅŖ(qi©óng)╬³╩šŻ¼E1Ą─╬³╩šÄ¦╩Ūė^▓ņ▓╗ĄĮĄ─Ż¼«ö(d©Īng)▒ĮŁh(hu©ón)╔Žėą░l(f©Ī)╔½╗∙łF(tu©ón)Ūę┼c▒ĮŁh(hu©ón)╣▓▄ŚĢr(sh©¬)Ż¼E2Ą─╬³╩šÄ¦│Ż║═K╬³╩šÄ¦║Ž▓óŻ¼╬³╩šĘÕŽ“ķL▓©ęŲäė(d©░ng)Ż©▒Įęę═¬Ż¼K 240nmŻ¼13000Ż╗B 278nmŻ¼1100Ż╗R 319nm Ż¼59Ż®
╣▓▄Ś¾wŽĄ┼c╬³╩šÄ¦▓©ķLĄ─ĻP(gu©Īn)ŽĄ
ų╗║¼╣┬┴óļpµIĄ─╗»║Ž╬’╚ńęꎮŻ¼Ųõ”ą ”ą*▄S▀wĄ─╬³╩š▓©ķL╠Äė┌šµ┐šūŽ═Ōģ^(q©▒)ĪŻ╚ń╣¹ėąā╔éĆ(g©©)╗“ČÓéĆ(g©©)ļpµI╣▓▄ŚŻ¼ät”ą ”ą*▄S▀wĄ─╬³╩š▓©ķLļS╣▓▄Ś│╠Č╚į÷╝ėČ°į÷╝ėŻ¼▀@ĘN¼F(xi©żn)Ž¾ĘQ×ķ╣▓▄Ś╝tęŲĪŻ▒Ē1┴ą│÷┴╦ę╗ą®╣▓▄ŚŽ®¤NĄ─╬³╩š╣ŌūV╠žš„ĪŻÅ─▒Ēųą┐╔ęį┐┤│÷├┐į÷╝ėę╗éĆ(g©©)╣▓▄ŚļpµIŻ¼╬³╩š▓©ķL╝sį÷╝ė40nm«ö(d©Īng)ļpµIöĄ(sh©┤)▀_(d©ó)ĄĮ7Ģr(sh©¬)Ż¼╬³╩š▓©ķLīó▀M(j©¼n)╚ļ┐╔ęŖ╣Ōģ^(q©▒)ĪŻ
| ╗»║Ž╬’ | ”ą ”ą*▄S▀wŻ©”╦/nmŻ® | ─”Ā¢╬³╣ŌŽĄöĄ(sh©┤) |
| ęꎮ 1,3-ČĪČ■Ž® 1,3,5-╝║╚²Ž® Č■╝ū╗∙ą┴╦─Ž® ╣’╬ÕŽ® | 170 217 256 296 335 | 1.5Ī┴104 2.1Ī┴104 3.5Ī┴104 5.2Ī┴104 11.8Ī┴104 |
▒Ē1 ─│ą®╣▓▄ŚŽ®¤NĄ─╬³╩š╠žš„
▓╗═¼Ą─░l(f©Ī)╔½╗∙łF(tu©ón)╣▓▄Śę▓Ģ■(hu©¼)ę²Ų”ą ”ą*▄S▀w╬³╩š▓©ķL╝tęŲĪŻ╚ń╣¹╣▓▄Ś╗∙łF(tu©ón)ųą▀Ć║¼ėąnļŖūėŻ¼ätn ”ą*▄S▀w╬³╩š▓©ķLę▓Ģ■(hu©¼)ę²Ų╝tęŲŻ©ęę╚®”ą ”ą*Ż¼170nm n ”ą*Ż¼290nmŻ╗▒¹Ž®╚®Ęųūėųąė╔ė┌┤µį┌ļpµI┼c¶╩╗∙╣▓▄ŚŻ¼”ą ”ą*Ż¼210nmŻ¼n ”ą*Ż¼315nmŻ®ĪŻ
╣▓▄Ś╩╣╬³╩šÄ¦▓©ķL╝tęŲŻ¼┐╔ęįšJ(r©©n)×ķ╩Ūė╔ė┌╣▓▄Śą╬│╔┴╦░³└©╣▓▄Ś╠╝įŁūėų«ķgĄ─ļxė“”ąµIŻ¼”ąļŖūėĖ³╚▌ęū▒╗╝ż░l(f©Ī)Č°▄S▀wĄĮĘ┤µI”ą▄ēĄ└╔ŽĪŻ└²╚ńČĪČ■Ž®Ęųūėųą├┐éĆ(g©©)╠╝įŁūėĄ─PzļŖūė┐╔ęįĮM│╔╦─éĆ(g©©)ĘŪČ©ė“Ęųūė▄ēĄ└Ż¼╝┤ā╔éĆ(g©©)│╔µI”ą▄ēĄ└”ą1Īó”ą2║═ā╔éĆ(g©©)Ę┤µI”ą▄ēĄ└”ą3*Īó”ą4*Ż¼╚ńłD2╦∙╩ŠĪŻ«ö(d©Īng)ČĪČ■Ž®Ęųūė╩▄ĄĮūŽ═Ō╣Ō╝ż░l(f©Ī)Ģr(sh©¬)Ż¼╠Äė┌”ą2▄ēĄ└╔ŽĄ─ļŖūėų╗ąĶĮė╩▄▌^Ą═Ą──▄┴┐Š═┐╔ęį▄S▀wĄĮ”ą3*▄ēĄ└╔ŽŻ¼▀@Š═ī¦(d©Żo)ų┬╬³╩šÄ¦▓©ķL╝tęŲĪŻ
¶╩╗∙┼cŽ®ļpµI╣▓▄Ś▓╗Ą½╩╣ļŖūėį┌│╔µI”ą▄ēĄ└┼cĘ┤µI”ą▄ēĄ└ų«ķg▄S▀wĄ──▄┴┐ĮĄĄ═Ż¼ę▓╩╣n ”ą*▄S▀wĄ──▄┴┐ĮĄĄ═Ż¼╚ńłD4╦∙╩ŠĪŻĘŪ╣▓▄ŚļpµI▓╗Ģ■(hu©¼)ė░Ēæ╬³╩šÄ¦Ą─▓©ķLŻ¼Ą½ī”(du©¼)╬³╩šÄ¦ÅŖ(qi©óng)Č╚ėąį÷╔½ą¦æ¬(y©®ng)ĪŻ
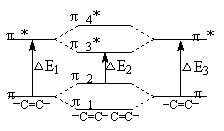
łD2 ╣▓▄ŚļpµI─▄╝ē(j©¬)łD

łD3 ¶╩╗∙┼cŽ®ļpµI╣▓▄Ś─▄╝ē(j©¬)łD

